Unidad 1 – Página 17
TIC
Regulación del ciclo
|
Conocer la existencia de señales que influyen en la progresión del ciclo |
|
|
Conocer la existencia de un «reloj molecular» y comprender los «engranajes» que lo mueven |
|
|
Observar y seguir el diagrama de interacciones moleculares |
|
|
Conocer el fenómeno de apoptosis |
|
Presentar direcciones de la WWW donde se puede ampliar los temas u obtener otro punto |
Regulación del ciclo celular

Las células proliferan aumentando su contenido de moléculas y orgánulos (crecimiento en masa o tamaño) y duplicando y segregando sus cromosomas, para posteriormente dividirse en dos células hijas que son genéticamente iguales. La proliferación celular tiene lugar de un modo controlado de acuerdo a las necesidades generales del organismo.
La regulación del ciclo celular ocurre de diferentes formas. Algunas se dividen rápidamente, otras como las células nerviosas pierden la capacidad de dividirse una vez que llegan a la madurez. Algunas, como las células hepáticas, conservan, aunque no la utilizan, su capacidad de división. Las células del hígado se dividen si se remueve parte del hígado y su división continúa hasta que el hígado retorna a su tamaño normal.
Factores ambientales tales como cambios en la temperatura y el pH, disminución de los niveles de nutrientes llevan a la disminución de la velocidad de división celular.
Reloj molecular

Basados en las investigaciones realizadas en huevos de anfibios los investigadores imaginaron la existencia de un «reloj central bioquímico» u oscilador que «instruye» a los núcleos acerca de las funciones a cumplir para controlar las fases de la división.
Todas la células eucariotas tienen un «reloj molecular» que determina cuando debe dividirse. Para programar estos sucesos el «reloj del ciclo celular» se vale de diversas moléculas proteicas. Los dos » engranajes» moleculares de este reloj son:
|
las ciclinas |
|
|
las quinasas (las CDK) |
En el control de la división celular intervienen dos tipos de moléculas:
|
CICLINAS: llamadas así porque alternan períodos de síntesis con períodos de degradación. Se reconocen dos: |
|||||
|
QUINASAS (CDK) dependientes de las ciclinas: actúan cuando son activadas por la ciclinas fosforilando moléculas cruciales para la división celular. En los seres superiores se identificaron dos principales:
|
Estos «engranajes» se asocian entre sí e inician los «movimientos» que llevan a iniciar los diferentes estadios del ciclo celular. Por ejemplo en la G1 temprana las ciclinas del tipo D se unen a la CDK4 o CDK6 y el complejo resultante «libera» el freno que impedía la progresión hacia la G1 tardía y, por lo tanto, el pase a la fase S (el complejo ciclina D- CDK4/6 desarma un potente inhibidor de la progresión del ciclo: el formado por la proteína pRB y los factores de transcripción inactivos). La progresión del ciclo depende en gran medida de que se alcancen niveles elevados de ciclinas, a saber en la siguiente secuencia:
-
Ciclina D
-
Ciclina E
-
Ciclina A
-
Ciclina B
Activación de la división celular

Para que la célula abandone la fase G1 e ingrese a la fase S, es decir inicie la replicación del ADN, la ciclina G1 aumenta su concentración a partir del punto R y activa la quinasa cdk2. A partir de este momento ambas moléculas proteicas conforman un FACTOR PROMOTOR DE LA REPLICACIÓN (FPR) que activa la síntesis del ADN. Cuando la concentración de ciclina decrece la cdk2 se libera y el complejo FPR se desactiva. Los niveles de cdk2 son constantes todo el ciclo.
Superada la fase G2, se activa el inicio de la mitosis. Al final de la G2 aumenta la concentración de ciclina mitótica y al alcanzar una determinada concentración se une a la cdc2 componiendo el FACTOR PROMOTOR DE LA (FPM) que se encarga de fosforilar proteínas con funciones esenciales durante la mitosis. Cuando todos los cinetocoros se han ligado a las fibras del huso se desactiva este complejo.
El punto R

Un instante crucial del ciclo es el que ocurre en el punto R (por restrictivo) de la fase G1 momento en el cual la célula decide si debe o no avanzar en la prosecución del ciclo. La «llave» de este paso es un conmutador molecular que pasa de «apagado» a «encendido».
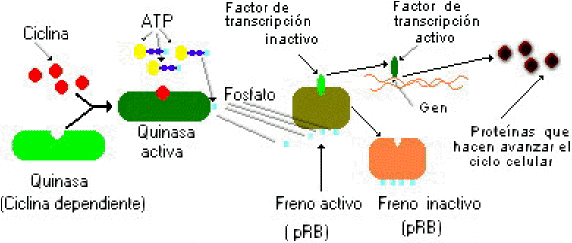 |
| El esquema muestra la forma en que ocurre esta conmutación: |
| Las ciclinas D y E aumentan su nivel | |
| A medida que sube el nivel de las ciclinas, las mismas se combinan con quinasas dependientes de ciclinas (es decir enzimas fosforilantes cuya actividad depende de los niveles de ciclinas). | |
| Las quinasas activas transfieren fosfatos del ATP a la proteína pRB (el «freno» del ciclo celular) | |
| Si la pRB no esta fosforilada «secuestra» (es decir permanece unida) a otras proteínas claves para la prosecución del ciclo: los factores de transcripción, en otras palabras, mantiene la llave en «apagado». | |
| Cuando el complejo ciclina-quinasa añade suficientes fosfatos a la pRB, la misma libera los factores de transcripción que actúan sobre los genes | |
| Los genes estimulados producen proteínas necesarias para que avance el ciclo celular |
En los vertebrados el franqueo del punto R esta regulado por los factores de crecimiento que se unen a los receptores de la superficie celular. Esto produce una «cascada» de reacciones destinadas a activar quinasas mitogénicas que migran al núcleo y fosforilan las proteínas. Estas últimas, que controlan los genes de proteínas (valga la redundancia) implicadas en la división celular (ciclinas), son las que desencadenan la mitosis.
Estímulos externos

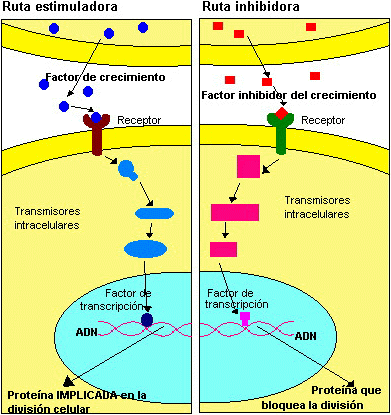 |
Las células normales se reproducen en respuesta a una «cascada» de señales que les envían los factores de crecimiento externos y detienen su división en respuesta a factores inhibidores que, obviamente, actúan también por medio de una cascada de señales.
Las sustancias inductoras externas pueden provenir de células vecinas: secreción paracrina, o de grupos celulares distantes (secreción endócrina). Estas sustancias actúan a nivel del punto de control G1, activan la síntesis de ciclinas y esta la de la fase S.
Sustancias inductoras de la proliferación celular:
|
Factores de crecimiento: en su mayoría son de secreción paracrina, algunos son los factores de crecimiento fibrobásticos FGF, plaquetarios PDGF y epidérmico EGF, que estimulan la proliferación de muchos tipos celulares. |
|
|
SOMATOMEDINA: estimula la proliferación de células cartilaginosas durante el crecimiento óseo. Esta sustancia se sintetiza en el hígado en respuesta a la hormona de crecimiento hipofisiaria. |
|
|
ERITROPOYETINA: originada por secreción endócrina en los riñones, estimula la proliferación de glóbulos rojos en la médula ósea. |
Frenos a la división celular

Un importante regulador del ciclo celular lo constituye una proteína denominado p53, la cual por un lado ejerce un control de tipo negativo frenando la división a nivel de G1, antes de punto R. Esta proteína es sintetizada por la propia célula en respuesta a la aparición de alteraciones del ADN, se origina en el gen p53 perteneciente a la categoría de genes supresores de tumores.
La p53 hace que se expresen otros genes de proteínas reguladoras como los p21 y p16 que bloquean la actividad de la cdk2. Las células, al no replicar su ADN se estabilizan en la fase G1. Si el ADN replicado tiene un daño peligroso para las células hijas, la proteína p53 se encarga de la muerte celular o apoptosis (muerte celular programada).
Resulta interesante señalar que aquellos fármacos anticancerígenos que actúan alterando, de alguna manera, la replicación correcta del ADN requieren, para su completa efectividad, una p53 funcionante. Pueden, si esto se cumple, desencadenar la apoptosis de las células cancerosas alteradas por el fármaco.
Existen otras importantes proteínas reguladoras de la proliferación celular, una de ellas es la Rb (por el tumor de retina denominado retinoblastoma) deriva del gen Rb, que también es supresor de tumores.
Por otra parte, diversas proteínas reprimen el ciclo al actuar como inhibidores.
|
Las proteínas p15 y p16 bloquean la actividad del complejo CDK-ciclina D (recuerde que esta quinasa en su forma activa activa la pRB) e impiden que el ciclo progrese de G1 a S. |
|||||||||
|
Otro inhibidor de CDK, la proteína p21 actúa a lo largo de todo el ciclo celular |
|||||||||
|
La p21 esta bajo el control de la denominada:
|
Telómeros

Es necesario señalar que existe un mecanismo destinado a «contar» el número de duplicaciones de una población celular, el mismo se encuentra presente en los extremos de los cromosomas en los segmentos denominados telómeros, estos telómeros se acortan un poquito cada vez que el cromosoma se replica. Cuando la disminución sobrepasa cierto límite suena una «alarma» que hace que las células entren en senescencia.
Durante cada ciclo de división celular se produce un acortamiento (se pierden unos 50-200 nucleótidos) de los extremos de los cromosomas, llamados telómeros. Ello se debe a la incapacidad de la DNA polimerasa de replicar los extremos de las moléculas de DNA. Hoy se cree que este mecanismo es parte del «reloj» celular que cuenta el número de divisiones y es responsable de la limitación de la vida de las células. Al llegar a un punto crítico de acortamiento de los telómeros las células entran en un proceso de senescencia y pierden la capacidad de dividirse.
La telomerasa es un complejo constituido por un RNA y varias proteínas que evita el acortamiento de los telómeros. No es el único mecanismo, pero posiblemente sí el más importante. La telomerasa es muy activa en células fetales, que mantienen un alto nivel de proliferación, pero muy poco en células de los tejidos en adultos. La observación de que las células tumorales expresan niveles elevados de telomerasa ha llevado a especular que su reactivación puede ser necesaria para el crecimiento tumoral, y que su inhibición podría suponer un nuevo tipo de terapia contra el cáncer. El mantenimiento de los telómeros juega un papel importante en la inmortalización de las células, como se deduce de la observación de que ratones que carecen de telomerasa muestran un acortamiento de su vida, algunos síntomas de envejecimiento prematuro, una menor capacidad de cicatrización de heridas, y una mayor incidencia de cánceres. Aunque por sí sola no causa transformación de células normales en cancerosas, la reactivación de la telomerasa coopera durante tumorogénesis con mutaciones en oncogenes como ras y genes supresores como p53 y Rb.
La eliminación de la telomerasa, y por tanto el acortamiento de los telómeros, causa inestabilidad cromosómica, errores en la segregación y aparición de anomalías y diversos tipos de mutaciones. En esta situación, la inducción del gen supresor p53 parece ser importante para provocar la muerte celular y evitar así la acumulación de mutaciones y malignización de las células. Si la expresión de p53 se anula por mutación se produce lo que se ha denominado la catástrofe genética, con masiva acumulación de mutaciones.
Apoptosis

La muerte de las células puede producirse por múltiples causas, como daño mecánico, infección por virus u otros microorganismos, acción de agentes químicos tóxicos o por acumulación de sustancias de desecho.
La muerte puede darse por dos mecanismos:
-
Necrosis: las células se hinchan y sufren un deterioro de su estructura y organización, así como el progresivo cese de sus funciones (síntesis de proteínas y ácidos nucléicos, respiración…) que acaba por impedir su viabilidad y conduce a la rotura de la membrana externa y la lisis. Ello ocasiona la liberación de material celular al medio, que suele provocar a su vez reacciones inflamatorias.
-
Apoptosis o muerte celular programada: este segundo tipo de muerte celular implica la activación de mecanismos específicos que conducen a la muerte de las células, siendo un fenómeno mucho más común de lo que puede pensarse. Se produce de modo natural durante el desarrollo embrionario y postnatal temprano en múltiples tejidos. Su función puede ser la eliminación de células superfluas en un lugar determinado. Durante el ciclo celular, se produce apoptosis mediada por el gen supresor p53 u otros mecanismos cuando el DNA que va a ser o está siendo replicado presenta alteraciones, evitándose así la generación de células anormales.
Cuando una célula normal completa su función fisiológica o percibe un daño genético o celular pone en funcionamiento un proceso fisiológico denominado apoptosis que induce su propia muerte. En este proceso parece intervenir (entre otros) un ![]() (Apoptosis Inducing Factor) factor inductor de la apoptosis que se encuentra en las mitocondrias y que al desencadenarse el proceso migra hacia el núcleo provocando la destrucción del ADN.
(Apoptosis Inducing Factor) factor inductor de la apoptosis que se encuentra en las mitocondrias y que al desencadenarse el proceso migra hacia el núcleo provocando la destrucción del ADN.
|
|
|
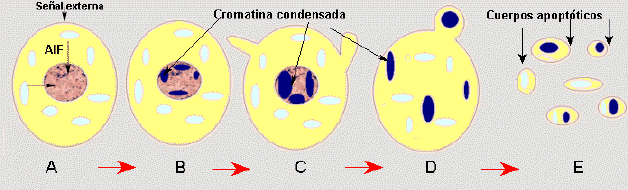
Este esquema sintetiza los cambios morfológicos que acontecen en una célula que sufre apoptosis |
A. Célula normal con orgánulos en su citoplasma y un núcleo con su cromatina heterogénea
B. Comienzo de la compactación de la cromatina
C. Gran condensación de la cromatina, protuberancias en la superficie celular.
D. Desaparece la membrana nuclear y se observan formas esféricas u ovoides de cromatina condensada.
E. La célula comienza a fraccionarse en los denominados cuerpos apoptóticos(componentes citoplasmáticos y nucleares rodeados por membrana plasmática). Célula fragmentada en cuerpos apoptóticos, estos cuerpos son eliminados por las células fagocitarias (que en realidad comienza en una etapa mas temprana.
Resulta interesante señalar que algunos autores consideran como células tumorales a aquellas que «pueden soportar ciertos daños genéticos que en una célula normal inducirían su propia muerte celular por un proceso fisiológico denominado apoptosis«, a diferencia de quienes las consideran únicamente como células de proliferación incontrolada y esto puede resultar de gran importancia para el diseño de agentes quimioterápicos.
La mayor parte de los agentes empleados en quimioterapia anticancerosa basan su acción en la producción de roturas y/o alteraciones en el DNA de las células. De este modo, inducen el fenómeno de apoptosis y la muerte de las células tumorales. Desgraciadamente, una de las causas de fallo de los tratamientos quimioterápicos es la aparición de resistencias a la muerte apoptótica de las células tumorales como consecuencia de la mutación de genes como p53.
|
Bases moleculares de la apoptosis:http://www.raf.es/pdf/anales/2003/vol1/M.%20Cascales.pdf |
|
|
Apoptosis: http://www.cnio.es/es/cancer/cap802.htm |
Regulación y Cáncer

El Cáncer consiste en el crecimiento descontrolado y diseminación de células anormales en el organismo, que invaden y dañan tejidos y órganos. El cáncer es la segunda causa de muerte en los países desarrollados, en los que una de cada cuatro personas fallece debido a esta enfermedad.
Todos los cánceres se originan como consecuencia de cambios llamados mutaciones en los genes de nuestras células. El cáncer es, por tanto, una enfermedad genética. Sin embargo, generalmente no es hereditaria. Es decir, que salvo un pequeño porcentaje, el cáncer no se transmite de padres a hijos.
El cáncer se inicia cuando una célula escapa a los controles de división y muerte celular y comienza a proliferar descontroladamente. Todas las células de un tumor, benigno o maligno, derivan de una sóla célula: es decir, los tumores son monoclonales.
La carcinogénesis o aparición de un cáncer es el resultado de dos procesos sucesivos:
|
el aumento descontrolado de la proliferación de un grupo de células que da lugar a un tumor o neoplasia, y |
|
|
la posterior adquisición por estas células de capacidad invasiva, que les permite diseminarse desde su sitio natural en el organismo y colonizar y proliferar en otros tejidos u órganos (proceso conocido como metástasis). |
Si sólo tiene lugar un aumento del crecimiento de un grupo de células en el lugar donde normalmente se hallan, se habla de un tumor benigno, que generalmente es eliminable completamente por cirugía. Por el contrario, cuando las células de un tumor son capaces de invadir los tejidos circundantes o distantes, tras penetrar en el torrente circulatorio sanguíneo o linfático, y formar metástasis se habla de un tumor maligno o cáncer.
Existen genes que en sus versiones «sanas» están relacionados con el control de crecimiento y supervivencia celular, que en otras circunstancias están relacionados con la aparición de ciertos tipos de cánceres. Entre ellos se encuentran:
|
Protooncogenes: genes normales que estimulan la proliferación celular. Su versión alterada se denomina Oncogen que dan lugar a la excesiva y descontrolada proliferación celular |
|
|
Genes supresores de tumores: inhiben la producción anormal de células. Un defecto en estos genes al eliminar los frenos naturales generan cuadros cancerosos. |
Interacciones moleculares

|
|
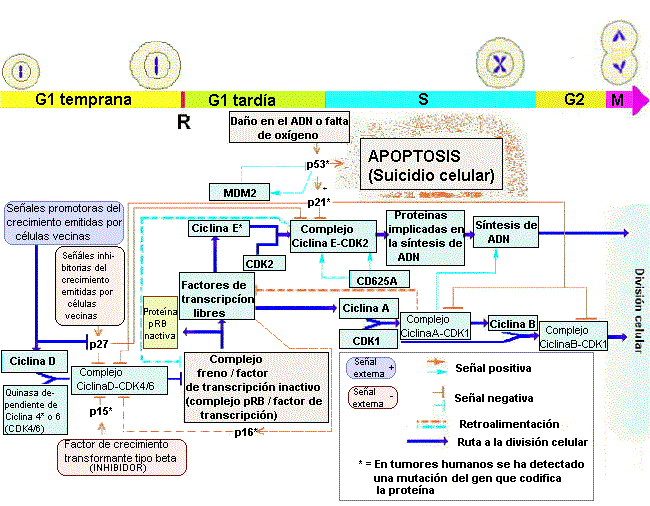
El esquema muestra las múltiples interacciones moleculares en el curso del ciclo celular. Mas allá del punto R se observa los cambios que ocurren para mantener el conmutador en «encendido».
|
El Genoma Humano Plantas y Animales Transgénicos Terapia Génica |
|
| Guía sobre el Ciclo Celular y Mitosis http://www.biologia.arizona.edu/cell/tutor/mitosis/09q.html | |
| O Ciclo Celular, uma Breve Introdução http://www.icb.ufmg.br/~lbcd/grupo1/ciclo.html |
Muñoz. (20 de febrero de 2008). Regulación del ciclo. Hipertextos del Área de Biología. Recuperado de http://goo.gl/lbNqpI